Lo nuevo
La Catástrofe Ultravioleta y el infinito (parte III)

La Catástrofe Ultravioleta y el infinito (parte II)

La Catástrofe Ultravioleta y el infinito (parte I)





En el artículo sobre el rubidio del mes pasado mencioné el hecho de que hay relojes atómicos que emplean transiciones energéticas entre niveles de la estructura hiperfina del rubidio-87 para medir el tiempo. Juan Carlos preguntó entonces qué era eso de la estructura hiperfina, de modo que aquí tenéis la respuesta en forma de un breve artículo.
Como ha pasado otras veces, haber leído otros artículos antes puede ayudar mucho a entender éste, pero intentaré ir mencionándolos según sean relevantes. Además, no quiero entrar en una gran profundidad en esto porque inevitablemente saldrá según vayamos avanzando en la serie de los Premios Nobel. Esta entrada pretende ser entonces una explicación básica –con todas las limitaciones habituales, “Antes simplista que incomprensible”, si eres físico no leas este artículo, bla bla bla– para entender qué demonios es la estructura hiperfina.
Eso sí, por más que sea una explicación simple, es de cierta abstracción y entenderla requiere algo de esfuerzo; sobre todo requiere paciencia, porque tendremos que repasar algunos conceptos antes de llegar al de la estructura hiperfina. ¿Tienes un rato?
Para entender la existencia de la estructura hiperfina, antes de descender al mundo atómico parémonos un momento en el concepto de energía en nuestro mundo macroscópico. Te recomiendo, si no lo has leído aún, que eches un vistazo primero al artículo sobre la energía potencial dentro del bloque de Mecánica Clásica I.
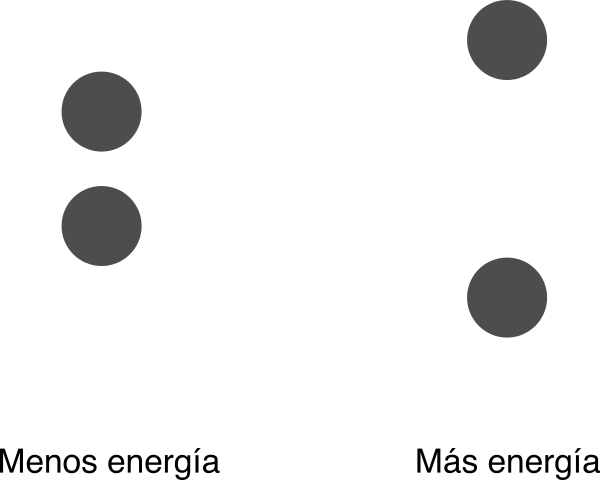
Imagina dos situaciones: dos planetas bastante cercanos el uno al otro, y los mismos dos planetas más alejados el uno del otro. Esos dos sistemas no tienen la misma energía – podemos pasar muy fácilmente del segundo al primero, pero nos costaría mucho más hacerlo al revés. El criterio que seguimos en física, por cierto, es decir que el sistema formado por los planetas tiene menos energía en el primer caso, y más energía en el segundo. Sé que esto puede resultar obvio, pero no tenerlo claro haría inútil el resto del artículo.
En casi cualquier otra situación en la que hay involucradas fuerzas podemos hacer lo mismo: si hay dos situaciones en las que esas fuerzas tienden a llevar el sistema de una a la otra, la primera tiene más energía que la segunda, y esa transición de la primera a la segunda será espontánea. Para pasar de la segunda a la primera –como en el caso de nuestros planetas cercanos si queremos alejarlos– nos hará falta aportar energía al sistema en forma de trabajo.
Esto sucede también en los átomos. Así, si un electrón se encuentra muy cerca del núcleo atómico, será fuertemente atraído por él, ya que ambas cargas son de signos contrarios, mientras que un electrón muy alejado del núcleo será atraído más débilmente. Dicho en términos energéticos, el electrón cercano al núcleo tiene menos energía que el alejado del núcleo. Si has leído Cuántica sin fórmulas ya sabes además que no todas las energías son posibles para un electrón alrededor del núcleo; esas energías están cuantizadas, y cada escalón energético se denomina nivel. Hablamos de todo esto al hacerlo del modelo atómico de Bohr.
Cuando un electrón pasa de un nivel energético a otro –por ejemplo, acercándose al átomo desde un nivel más elevado– se dice que ha realizado una transición. Si recuerdas el ejemplo de los planetas, para que un electrón ascienda de nivel hará falta que alguien le proporcione energía, mientras que si cae a un nivel más cercano al núcleo será él quien emita energía. Hablamos de ello al hacerlo del efecto fotoeléctrico.
Si sólo pensamos en la energía que tiene un electrón orbitando el núcleo en términos de la atracción entre ambos, es evidente que dos electrones que están a la misma distancia del núcleo tendrán la misma energía: estarán en el mismo nivel. Es posible desdoblar este nivel en dos si rompemos la simetría, es decir, si añadimos algo al sistema que haga que alguna diferencia entre ambos electrones que no se traducía en una energía mayor o menor tenga una consecuencia energética.
Esto es lo que sucede precisamente con el efecto Zeeman, que supuso el Nobel de Física de 1902. Cuando se somete un átomo a un campo magnético externo razonablemente intenso –para que se note el efecto con claridad– aparece una diferencia entre electrones que estaban en el mismo nivel energético: un electrón que gira alrededor del átomo en un determinado plano no tendrá ya la misma energía que otro que gire en un plano diferente.
Como ejemplo extremo, imagina dos electrones que giran alrededor del átomo a la misma distancia, pero uno lo hace en sentido contrario al otro. Cada uno de los dos, al girar alrededor del núcleo, crea un campo magnético: cualquier carga eléctrica en movimiento lo hace, de acuerdo con la ley de Ampère-Maxwell. La dirección de ese campo magnético tiene que ver con la orientación de la órbita del electrón – no importa ahora hacia dónde va, sino simplemente que su dirección está determinada por la órbita.
Esto significa que nuestros dos electrones, girando en sentidos contrarios, crean sendos mini-campos magnéticos en sentidos contrarios. Esto daría exactamente igual, pero al someter el átomo a un gran campo magnético externo, aparece algo nuevo: la interacción entre el campo magnético del electrón y el campo externo. Es algo similar a si tienes un solo imán (el campo de un electrón), y no notas nada; pero, si aparece un segundo imán (el campo externo), entonces sí notas que hay una interacción entre ambos.
Imagina por lo tanto que el campo externo que introducimos va en la dirección de uno de los campos magnéticos de los electrones: el campo externo y el creado por ese electrón van “a favor” uno del otro, pero eso significa que el campo externo va “en contra” del campo del otro electrón. Inmediatamente te darás cuenta de la consecuencia energética: los dos electrones no tienen ya la misma energía. Es más fácil poner campos magnéticos a favor que en contra, como seguro que sabes si has intentado enfrentar dos imanes.
Si has entendido esto, vamos un poco más allá. Hasta ahora hemos considerado que –campos externos aparte– la única energía involucrada aquí es la debida a la atracción entre el núcleo y los electrones. Si bien esto no es cierto, sí lo es que la energía debida a esa atracción es con mucha diferencia la fundamental. Tanto es así que la estructura de niveles energéticos debida a ella se denomina a veces estructura gruesa. Podrías pensar en ella como una especie de “escalera energética” de grandes peldaños.
Pero no es la única.

La razón es justo la suposición que hemos hecho hasta ahora: que la única energía es la debida a la atracción núcleo-electrón. Ya hemos visto que existen otras posibles energías, como la debida a la orientación de la órbita atómica y el campo externo, pero ¿dónde aparecen éstas dentro del átomo?
Un lugar en el que lo hacen es el siguiente: hemos dicho que la órbita del electrón crea un campo magnético cuya dirección depende de la orientación de la órbita. Ahora bien, el electrón tiene un campo magnético propio, que en términos clásicos podríamos describir como el debido a la rotación sobre su propio eje: el espín. Es algo así como si la Tierra crease un campo magnético en su traslación alrededor del Sol, y otro en su rotación sobre el eje.
Pero entonces tenemos dos campos magnéticos diferentes, cuya orientación relativa puede determinar energías distintas. Dicho mal y pronto, si el campo de la órbita y el espín tienen el mismo sentido, la energía del electrón será menor que si tienen sentidos contrarios.
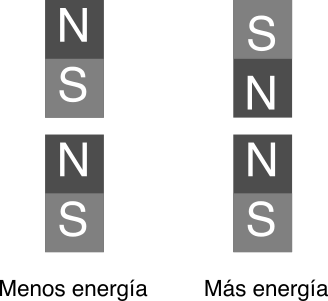
Ahora bien, la diferencia es minúscula. Piensa que la energía debida a la atracción entre el núcleo positivo y el electrón negativo es varios órdenes de magnitud mayor que la debida a estas sutilezas del campo magnético de la rotación del electrón – es un efecto muy pequeño. Es como si lo que pensábamos que eran escalones de nuestra “escalera energética” realmente no eran lisos, sino que tienen una estructura propia: cada peldaño no es raso, sino que tiene sub-peldaños muy pequeños.
Esta estructura energética secundaria dentro de la gruesa recibe el nombre de estructura fina. Involucrada en ella está además la relatividad, ya que los efectos relativistas debidos a la velocidad del electrón en su órbita son notables, pero la razón de ser de la estructura fina es la orientación relativa entre ambos campos magnéticos.
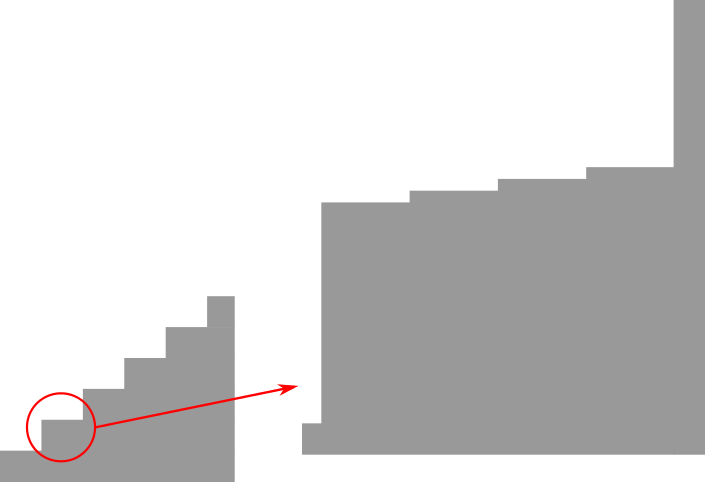
Pero la cosa no acaba aquí: incluso los minúsculos sub-escalones de la estructura fina no son lisos. ¡Hay otras fuentes de asimetría energética!
La razón es que no sólo los electrones tienen espín: los protones y los neutrones también. Esto significa que cada protón y cada neutrón también produce un campo magnético propio –en términos clásicos, debido a su rotación sobre el eje–. Sin embargo, el campo magnético creado por el núcleo a veces es nulo y siempre es pequeñísimo.
Como veremos tarde o temprano en la serie sobre los Premios Nobel, nuestro modelo del núcleo atómico –estupendamente bien apoyado por los experimentos– predice que los protones y los neutrones tienden a formar pares con espines opuestos, de modo que cada pareja de este tipo no produce un campo magnético externo, ya que ambos se cancelan. Si no hay un número par de nucleones, por supuesto, el campo magnético producido por el espín de protones y neutrones no es nulo, pero nunca será muy grande aunque haya muchos nucleones.
Ahora bien, si el núcleo tiene un número impar de nucleones –como pasa si sólo hay uno, como en el caso del hidrógeno con un protón y ningún neutrón, el protio– entonces existe un campo magnético nuclear debido al espín de esos nucleones. E imagino que sabes a dónde voy a parar…
La orientación relativa entre este campo magnético y los dos asociados al electrón –el debido a su órbita y el espín– determina niveles energéticos ligeramente diferentes.
Dicho de otro modo, la estructura fina no es el final del camino, sino que a su vez sus escalones se subdividen en otros aún menos profundos. La estructura fina era órdenes de magnitud menor que la gruesa, y este tercer grado de subdivisión, órdenes de magnitud menor que la estructura fina, se denomina estructura hiperfina.
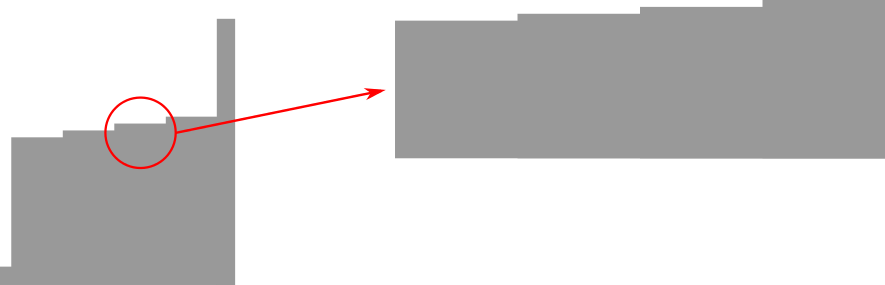
En el caso más simple de todos, imagina un átomo de protio con un protón y un electrón. Ese electrón podría (si adquiere energía) cambiar a un nivel energético mayor en la estructura gruesa, alejándose del átomo. O podría, sin cambiar su distancia al átomo, tener un espín en el mismo sentido que el campo orbital, o al contrario – dos niveles de la estructura fina. Pero también podría cambiar el espín del electrón respecto al espín del protón, haciendo que ambos campos magnéticos tuvieran el mismo sentido o no – otros dos niveles de la estructura hiperfina.
La cosa se puede complicar muchísimo más, por supuesto, y no estamos siquiera hablando de efectos relativistas, pero puedes ver la causa última de estas estructuras energéticas secundarias: son lo mismo que el efecto Zeeman, pero en vez de un campo magnético externo, se deben a las interacciones entre todos los campos magnéticos –más o menos intensos– producidos por las propias cargas subatómicas.
Ahora bien, si un electrón cambia entre dos niveles de la estructura gruesa, por ejemplo cayendo a un nivel inferior desde otro superior, la diferencia de energía es considerable. Esto significa que el electrón emitirá un fotón de cierta entidad, cargado de energía: por ejemplo, un fotón de radiación visible. Muchas excitaciones electrónicas son de este tipo, y los átomos brillan con luz propia.
Pero una transición dentro de la estructura fina es varios órdenes de magnitud menor: los niveles están tan cerca unos de otros que la diferencia de energía es muy pequeña. Un átomo nunca brillará con luz visible cuando un electrón cae de un nivel a otro dentro de la estructura fina: podrá hacerlo tal vez emitiendo un fotón en la región de las microondas.
Algo parecido pasa con una transición dentro de la estructura hiperfina: el fotón emitido tiene tan poca energía que nunca podría ser detectado a simple vista. El caso más famoso es el de la transición entre los dos niveles de la estructura hiperfina del estado fundamental del hidrógeno (espín del electrón y del protón en el mismo sentido o en sentidos opuestos), ya que alrededor del 90% de todos los átomos del Universo son de hidrógeno-1.
Entre esos dos niveles de la estructura hiperfina del hidrógeno hay una diferencia de energía minúscula: 9,4·10-25 julios. Sé que es difícil hacerse una idea de lo pequeñísimo de esta energía. Para que te hagas una idea, una simple molécula a -272 °C, tan sólo un grado por encima del cero absoluto, tiene una energía cinética quince veces mayor. Desde luego, un fotón de esa energía es invisible para el ojo humano. Su longitud de onda es de unos 21 cm, lo cual significa que es un fotón de microondas.

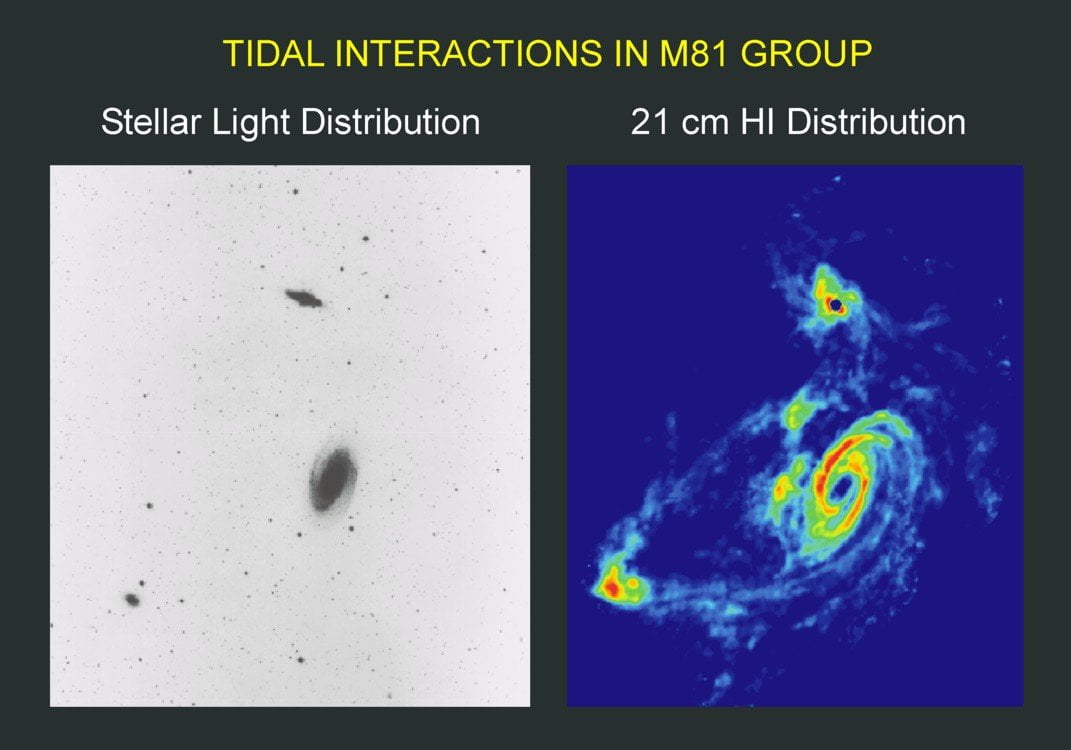
Sin embargo, que no podamos verlo no lo hace menos importante: la llamada línea de 21 cm es fundamental en astrofísica, ya que como he dicho antes prácticamente todo el Universo es hidrógeno. No sólo eso, sino que además las microondas son capaces de atravesar nubes de polvo y gas que la luz no puede atravesar, con lo que podemos obtener excelentes imágenes de regiones del Universo que no podríamos lograr usando luz. La radioastronomía hace uso de esa línea de la estructura hiperfina constantemente.
De hecho, la longitud de onda de los fotones de esta transición de la estructura hiperfina es una de las magnitudes básicas en el Universo. Tanto es así que Carl Sagan y Frank Drake la utilizaron como unidad de medida en las placas de oro transportadas por las sondas Pioneer 10 y 11. Las distancias allí empleadas, como las usadas al describir la altura de un ser humano, se expresan como múltiplos de la longitud de onda de esa transición.
Y, desde luego, estas transiciones en otros átomos, como el cesio, se utiliza para medir el tiempo en los relojes atómicos como describimos hace ya tanto tiempo al hablar del reloj; probablemente el final de aquel artículo tenga más sentido para ti ahora. Pero además del cesio se usan transiciones de la estructura hiperfina del rubidio-87 en otros relojes, lo cual provocó la duda de Juan Carlos que a su vez nos ha llevado a este ladrillo. El mundo es un lugar muy raro…
Para saber más (esta vez está todo en inglés porque no he encontrado nada comparable en castellano):
_______
Pedro Gómez-Esteban González. (2009). El Tamiz. Recuperado de: https://eltamiz.com/